Khí Sunfurơ là gì và các tính chất đặc trưng của khí Sunfurơ
Khí Sunfurơ được ứng dụng nhiều trong công nghiệp và đời sống. Tuy nhiên nó cũng là loại khí có rất nhiều tác hại. Vậy cùng chúng tôi đi tìm hiểu về loại khí này trong bài viết dưới đây nhé.
Nội dung tóm tắt
Khí sunfurơ là gì?
Khí sunfurơ tuyệt khí SO2 còn mang tên Call không giống là lưu hoàng dioxit (tốt còn được gọi là anhiđrit sunfurơ). Đây là sản phẩm thiết yếu khi đốt cháy lưu hoàng. SO2 (axit sunfurơ) được hiện ra nhờ vào quy trình đốt cháy những nguyên liệu hóa thạch nhỏng than, dầu, hoặc thổi nấu tung cá loại quặng Fe, nhôm, kẽm, chì.
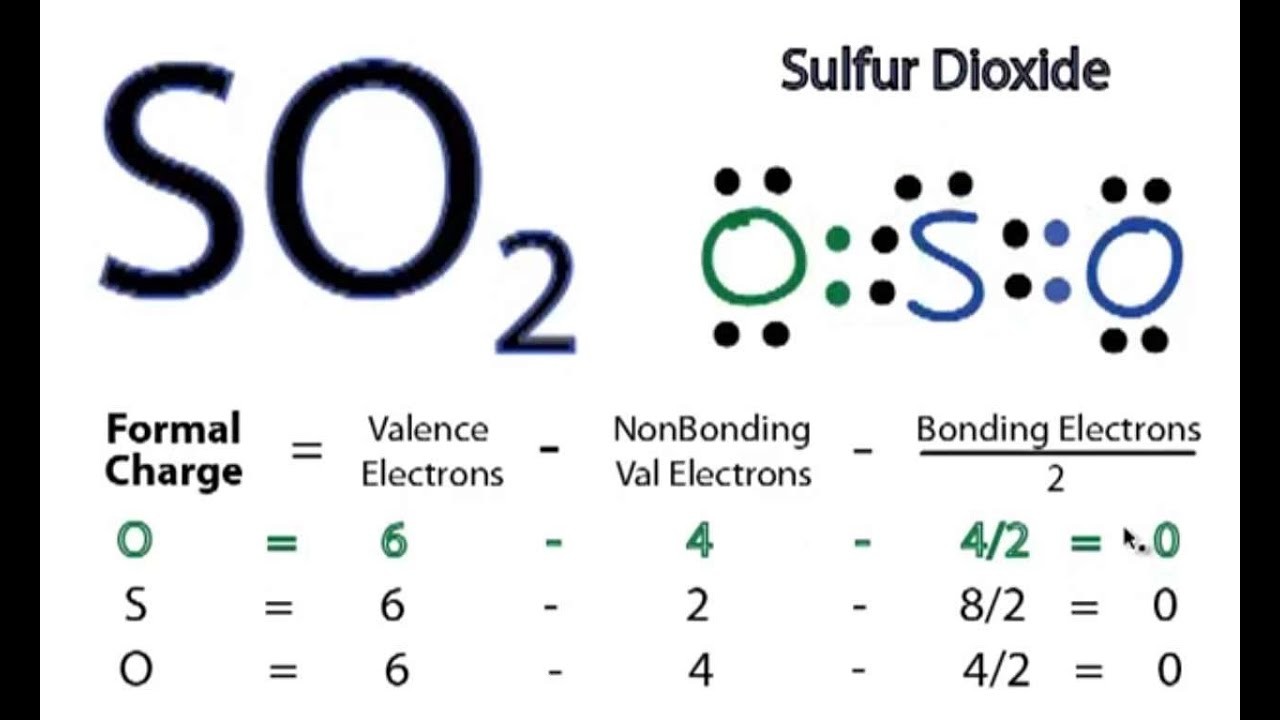
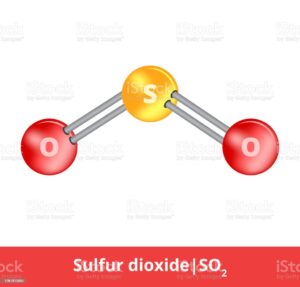
Cấu tạo phân tử và công thức cấu tạo
Nguyên tử lưu huỳnh bị kích thích có 4 electron chưa ghép đôi ở phân lớp 3p và 3d:… 3s2 3p3 3d1.
Các điện tử đơn độc này từ nguyên tử S sẽ liên kết với 4 điện tử đơn lẻ từ hai nguyên tử o để tạo thành bốn liên kết cộng hóa trị có cự.
Tính chất vật lý
Lưu huỳnh đioxit hay khí lưu huỳnh là chất khí không màu, không mùi, nặng gấp đôi không khí, hóa lỏng ở -10 ° C. Lưu huỳnh đioxit rất dễ tan trong nước (1 thể tích nước ở 20 ° C hòa tan được 40 ° C. Thể tích của khí so2 ). Lưu huỳnh đioxit là khí độc, hít thở không khí có khí SO2 sẽ bị viêm đường hô hấp.
Xem thêm: Khí rung là gì?
Tính chất hóa học
Lưu huỳnh đioxit là một oxit có tính axit
SO2 tan trong nước tạo thành dung dịch axit sunfuric (H2SO3).
Phương trình phản ứng
SO2 + H2O -> H2SO3
H2SO3 là một axit yếu (mạnh hơn axit sunfuric) và không bền (ngay cả trong dung dịch, dung dịch, H2SO3 cũng bị phân hủy thành SO2 và H2O).
SO2 phản ứng với các dung dịch bazơ, tạo thành hai loại muối: muối trung tính, chẳng hạn như Na2SO3, chứa các ion sunfit (SO3) và muối axit, chẳng hạn như NaHSO3, chứa các ion hydrosulfit (HSO3).
Lưu huỳnh đioxit là một chất oxi hóa trung gian
Trong hợp chất SO2, nguyên tố lưu huỳnh có số oxi hóa +4, là nguyên tố trung gian giữa số oxi hóa -2 và +6. Vì vậy, khi tham gia phản ứng oxi hóa khử, so2 có thể bị khử hoặc bị oxi hóa.
Lưu huỳnh đioxit dường như là một chất khử khi nó phản ứng với các chất oxi hóa mạnh, chẳng hạn như halogen, thuốc tím.
Phương trình phản ứng
5SO2 + 2KMnO4 + 2H2O -> K2SO4 + 2MnSO4 + 2H2SO4
Lưu huỳnh đioxit dường như là một chất oxy hóa khi nó phản ứng với các chất khử mạnh hơn, chẳng hạn như H2S, Mg, v.v.
Phương trình phản ứng
SO2 + 2H2S -> 3S + 2H2O
SO2 + 2Mg -> s + 2MgO
Các tác hại của khí Sunfurơ
Khí sunfuro đối với môi trường
- Đây là một chất khí gây ô nhiễm môi trường không khí.
- Lưu huỳnh đioxit bị oxy hóa và tác dụng với nước sẽ tạo ra axit sunfuric gây hiện tường mưa axit làm ảnh hưởng đến các loài động, thực vật khi tiếp xúc.
- Làm mỏng tầng ozon.
- SO2 cũng là một axit gây ăn mòn kim loại, bê tông trong điều kiện không khí ẩm. Các hiện tượng dễ nhận thấy nhất đó là gây rỉ sét cho sắt thép, thay đổi các tính chất vật lý màu sắc của đá vôi.
Khí sunfurơ gây hại cho sức khỏe con người
- Lưu huỳnh dioxit (SO2) và sunphua anhyđrit (SO3) trong tổ hợp các hạt lơ lửng và hơi ẩm rất có hại cho con người và các loại động vật.
- Khi hít phải khí sunfuro sẽ gây khó thở, nóng rát trong mũi và cổ họng… là nguyên nhân của bệnh viêm phổi, viêm đường hô hấp, viêm mắt…
- Khi tiếp xúc với da sẽ gây phù nề, phỏng thậm chí là hoại tử
- Khí sunfuro khi đi vào trong màu thông qua đường hô hấp hay tiêu hóa sẽ làm giảm khả năng vận chuyển oxy của các hồng cầu, làm nạn nhân rơi vào trạng thái khó thở.
Ứng dụng và điều chế khí sunfurơ

Xem thêm: Khí hậu 4 mùa ở Việt Nam như thế nào?
Lưu huỳnh đioxit được sử dụng để :
- Ứng dụng trong sản xuất axit sunfuric (H2SO4)
- vật liệu tẩy trắng: giấy, bột giấy, dung dịch đường…
- Ứng dụng SO2 trong nông nghiệp. sử dụng làm chất bảo quản cho những loại mứt quả sấy khô
- Là chất Kháng khuẩn và chống oxy hóa trong sản xuất rượu vang
Điều chế trong phòng thí nghiệm
Trong phòng thí nghiệm, SOHai được điều chế bằng cách đun nóng dung dịch axit HHaiSOBốn với muối NaHaiSOBa.
Thu SOHai vào bình bằng cách đẩy ko khí.NaHaiSOBa + HHaiSOBốn -> NaHaiSOBốn + HHaiO + SOHai
Điều chế trong công nghiệp
- Đốt cháy lưu huỳnh.
Đốt quặng sunfua kim loại, như pirit sắt (FeSHai) : 4FeSHai + 11OHai -> 2FeHaiOBa + 8SOHai
Hy vọng qua bài viết các bạn đã hiểu Khí sunfurơ là gì? Những tính chất đặc trưng cũng như tác hại của khí sunfurơ đối với sức khỏe con người. Chúc các bạn thành công.